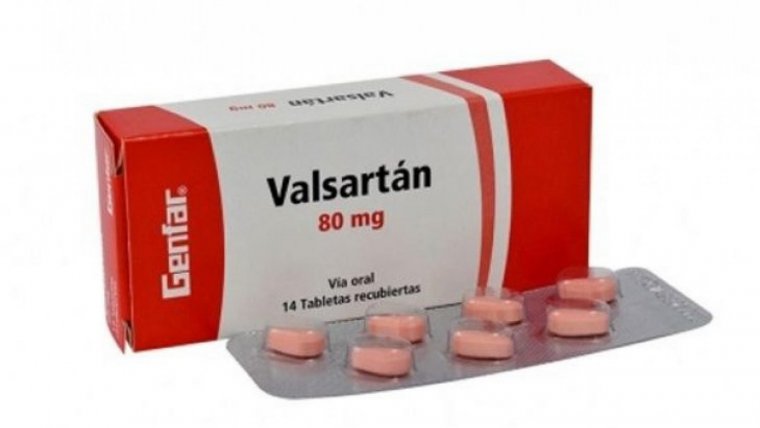

L'Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) ha tret del mercat 3 nous lots de medicaments després de comprovar que tenen valsartán, un principi actiu que s'utilitza per tractar la hipertensió, després dels que va retirar al juliol.
L'empresa xinesa Zhejiang Huahai Pharmaceutical és la que fabrica aquest principi actiu que perjudica els efectes del receptor de l'angiotensia-II. El passat 5 de juliol es va descobrir que aquest podria ser cancerigen a causa d'una impuresa que pot tenir.
Concretament aquests són els tres lots que es poden canviar gratuïtament per un altre fàrmac equivalent a les farmàcies:
- Valsartán Stada 160 mg comprimits recoberts amb pel·lícula EFG', 28 comprimits (NR: 72856, CN: 672649): Lot 64011, data de caducitat 25/10/2020.
- Valsartán Stada 320 mg comprimits recoberts amb pel·lícula EFG', 28 comprimits (NR: 72853, CN: 672639): Lot 71263V, data de caducitat 25/03/2021.
- Valsartán/ hidroclorotiazida Stada 160 mg/ 12,5mg comprimits recoberts amb pel·lícula EFG', 28 comprimits (NR: 73100, CN: 672877): Lot 64004, data de caducitat 25/10/2019.
Els primers lots es van retirar al juliol
Quan es va conèixer que aquests medicaments podien provocar càncer es van retirar tots els lots de les farmàcies. Les autoritats sanitàries de tota Europa van augmentar els seus controls i revisions d'aquest tipus de pastilles contra la tensió i van prohibir la venda de fàrmacs amb candesartán, irbesartán, losartán i olmesartán.
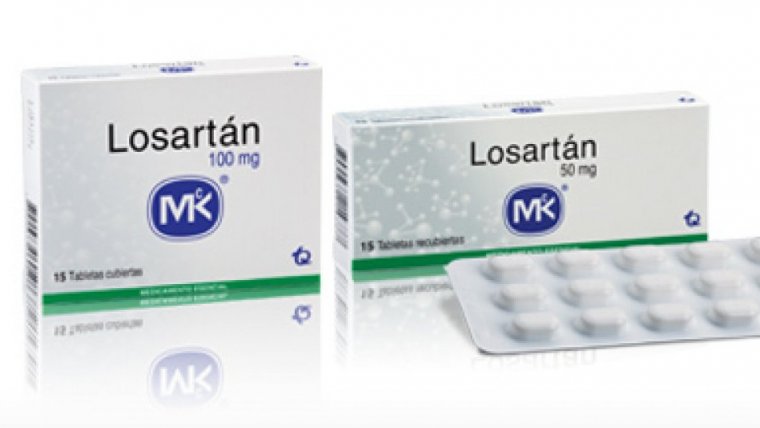
En un primer moment aquests no estaven en la llista de medicaments prohibits, però finalment un estudi fet a Alemanya va detectar els mateixos problemes d'impuresa en un losartán fabricat per l'empresa índia Hetero Labs. Aquesta mesura, però no va afectar Espanya perquè aquest producte no es comercialitza en les farmàcies de l'Estat.
L'empresa xinesa no pot produir més aquest medicament
L'alarma que ha generat la detecció d'aquest principi cancerigen en aquests medicaments contra el càncer ha fet que les autoritats europees realitzin una inspecció en les instal·lacions de Zhejiang Huahai Pharmaceutical a la ciutat xinesa Chuannan. Concretament ho ha fet la Direcció Europea de Qualitat dels medicaments.
Els resultats no van ser positius i es va demostrar que la companyia asiàtica incomplia les normes de fabricació. Per tant, se li va prohibir tornar a produir aquest tipus de principi actiu.

